Page 59 - IDITEC 2020
P. 59
Nº 9 – Año 2020 IDITEC ISSN: 2525-1597
Curiel y col. (2015) analizaron las poblaciones microbianas de masas de harinas de legumbres
italianas no fermentadas y fermentadas por L. plantarum C48 y L. brevis AM7. Estos autores reportaron
un número inicial de BAL de aproximadamente 1,0 a 2,5 log UFC/g, y hongos y levaduras en el orden de
1,1–3,5 log UFC/g para la mayoría de las harinas. En estas legumbres, la inoculación de las mismas con
los lactobacilos seleccionados permitió incrementar la población de BAL hasta 9,8–10,2 UFC/g al final
de la fermentación. Otros autores (Di Pasquale y col, 2020), emplearon también estas especies para
inocular harinas de legumbres (poroto, garbanzo, arveja y lenteja) y luego de 24 h de fermentación a 30°C
observaron un incremento de 2 log en la población de BAL en todas la harinas (densidad celular final de
9,54±0,05 a 9,82±0,09 log UFC/g).
.
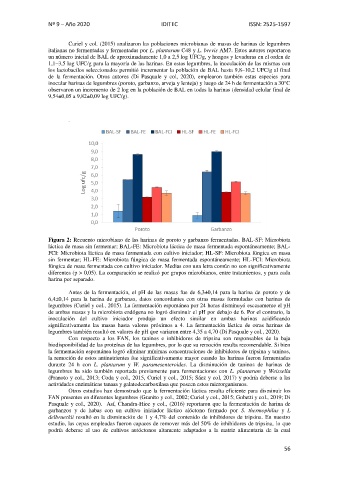
Figura 2: Recuento microbiano de las harinas de poroto y garbanzo fermentadas. BAL-SF: Microbiota
láctica de masa sin fermentar; BAL-FE: Microbiota láctica de masa fermentada espontáneamente; BAL-
FCI: Microbiota láctica de masa fermentada con cultivo iniciador; HL-SF: Microbiota fúngica en masa
sin fermentar; HL-FE: Microbiota fúngica de masa fermentada espontáneamente; HL-FCI: Microbiota
fúngica de masa fermentada con cultivo iniciador. Medias con una letra común no son significativamente
diferentes (p > 0,05). La comparación se realizó por grupos microbianos, entre tratamientos, y para cada
harina por separado.
Antes de la fermentación, el pH de las masas fue de 6,3±0,14 para la harina de poroto y de
6,4±0,14 para la harina de garbanzo, datos concordantes con otras masas formuladas con harinas de
legumbres (Curiel y col., 2015). La fermentación espontánea por 24 horas disminuyó escasamente el pH
de ambas masas y la microbiota endógena no logró disminuir el pH por debajo de 6. Por el contrario, la
inoculación del cultivo iniciador produjo un efecto similar en ambas harinas acidificando
significativamente las masas hasta valores próximos a 4. La fermentación láctica de otras harinas de
legumbres también resultó en valores de pH que variaron entre 4,35 a 4,70 (Di Pasquale y col., 2020).
Con respecto a los FAN, los taninos e inhibidores de tripsina son responsables de la baja
biodisponibilidad de las proteínas de las legumbres, por lo que su remoción resulta recomendable. Si bien
la fermentación espontánea logró eliminar mínimas concentraciones de inhibidores de tripsina y taninos,
la remoción de estos antinutrientes fue significativamente mayor cuando las harinas fueron fermentadas
durante 24 h con L. plantarum y W. paramesenteroides. La disminución de taninos de harinas de
legumbres ha sido también reportada previamente para fermentaciones con L. plantarum y Weissella
(Pranoto y col., 2013; Coda y col., 2015, Curiel y col., 2015; Sáez y col, 2017) y podría deberse a las
actividades enzimáticas tanasa y galatodecarboxilasa que poseen estos microrganismos.
Otros estudios han demostrado que la fermentación láctica resulta eficiente para disminuir los
FAN presentes en diferentes legumbres (Granito y col., 2002; Curiel y col., 2015; Gobetti y col., 2019; Di
Pasquale y col., 2020). Así, Chandra-Hioe y col., (2016) reportaron que la fermentación de harina de
garbanzos y de habas con un cultivo iniciador láctico alóctono formado por S. thermophilus y L
delbrueckii resultó en la disminución de 1 y 4,7% del contenido de inhibidores de tripsina. En nuestro
estudio, las cepas empleadas fueron capaces de remover más del 50% de inhibidores de tripsina, lo que
podría deberse al uso de cultivos autóctonos altamente adaptados a la matriz alimentaria de la cual
56